Stressfrakturer i sacrum
Av: Erik Iversen, Arne Larmo, Ina Garthe og Ellen Moen
Det antas at stressfrakturer i sacrum er en relativt sjelden skade. Insidensen er ukjent, men kan være så høy som 20% hos kvinnelige langdistanse løpere.3
I tillegg til skader hos løpere er det rapportert kasus fra idretter som tennis, basketball, turn, volleyball og friidrett.4Stressfrakturer i sacrum starter som i andre områder med resorpsjon av bein fulgt av beinmargsødem, som videre kan utvikle seg til en stressfraktur dersom belastningen opprettholdes.
Selve sacrum består av en midtre del og to sacrale ala, eller vinger.
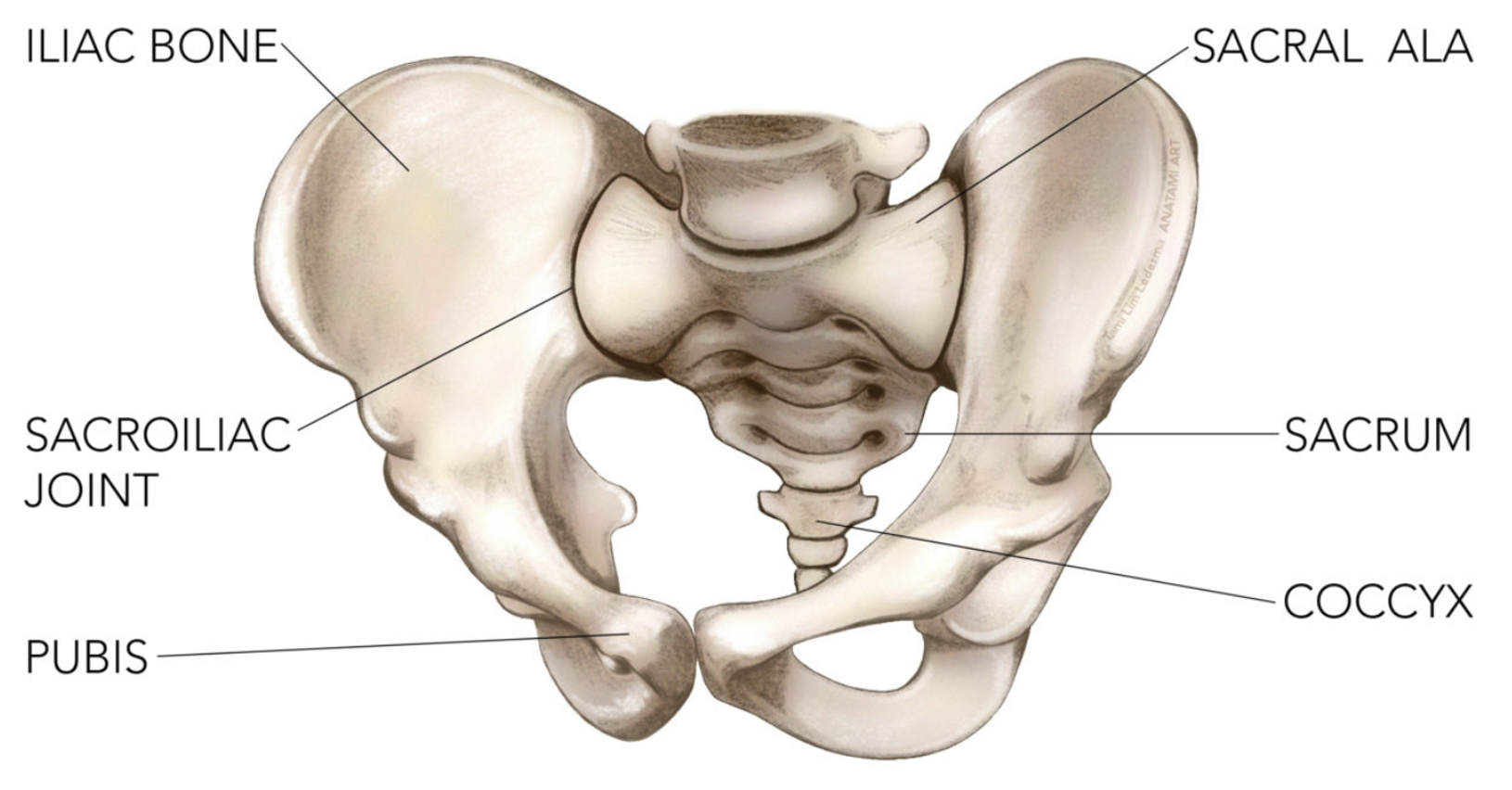
Sacrum er bredere kranialt og anteriort sammenlignet med de kaudale og posteriore beinoverflatene. Denne konstruksjonen gjør at sacrum kiler seg inn mot de motstående flatene på os ilium i aksial- og koronalplanet via iliosacralleddet (IS leddet).2
Under gange og løping er det unilaterale hemipelvis og sacrum understøttet av vekselvis høyre og venstre underekstremitet. Stabiliseringen av bekkenet over standbeinet utsetter de sacrale ala for maksimalt stress. Den ipsilaterale delen av sacrum bærer vekten av overkroppen og motsatt underekstremitet, sammen med en mindre stresskomponent mot den fremre bekkenringen. Belastningen på sacrum øker 145-207% under gange sammenlignet med to-beins aktivitet. Under gange i trapp og ved lett jogg øker de inferiøre kreftene fra virvelsøylen gjennom sacrum 400-500%.5
Biomekaniske modeller indikerer at fordelingen av krefter og stress på flate bein som sacrum kommer fra kortikalt bein. Kortikalt bein overfører kreftene fra én støttende region til en annen, mens det sentrale trabekulære beinet fungerer som støtte for å beholde avstanden mellom de kortikale overflatene.6
Sacrale stressfrakturer oppstår som følge av for stort stress fra vertikale krefter gjennom virvelsøylen som overføres til sacrum og de sacrale ala. Stressfrakturene oppstår som regel i en vertikal retning i sacral vingene, parallelt med IS-leddene. Ved videre progresjon av skaden kan det oppstå transversale sacrale frakturer. 3,7,8
Rehabiliteringen av stressreaksjoner/frakturer i sacrum krever avlastning og/eller redusert belastning. Øvelser i rehabiliteringsperioden må ta hensyn til at både de kortikale beinflatene og det trabekulære beinet ikke utsettes for stor belastning.
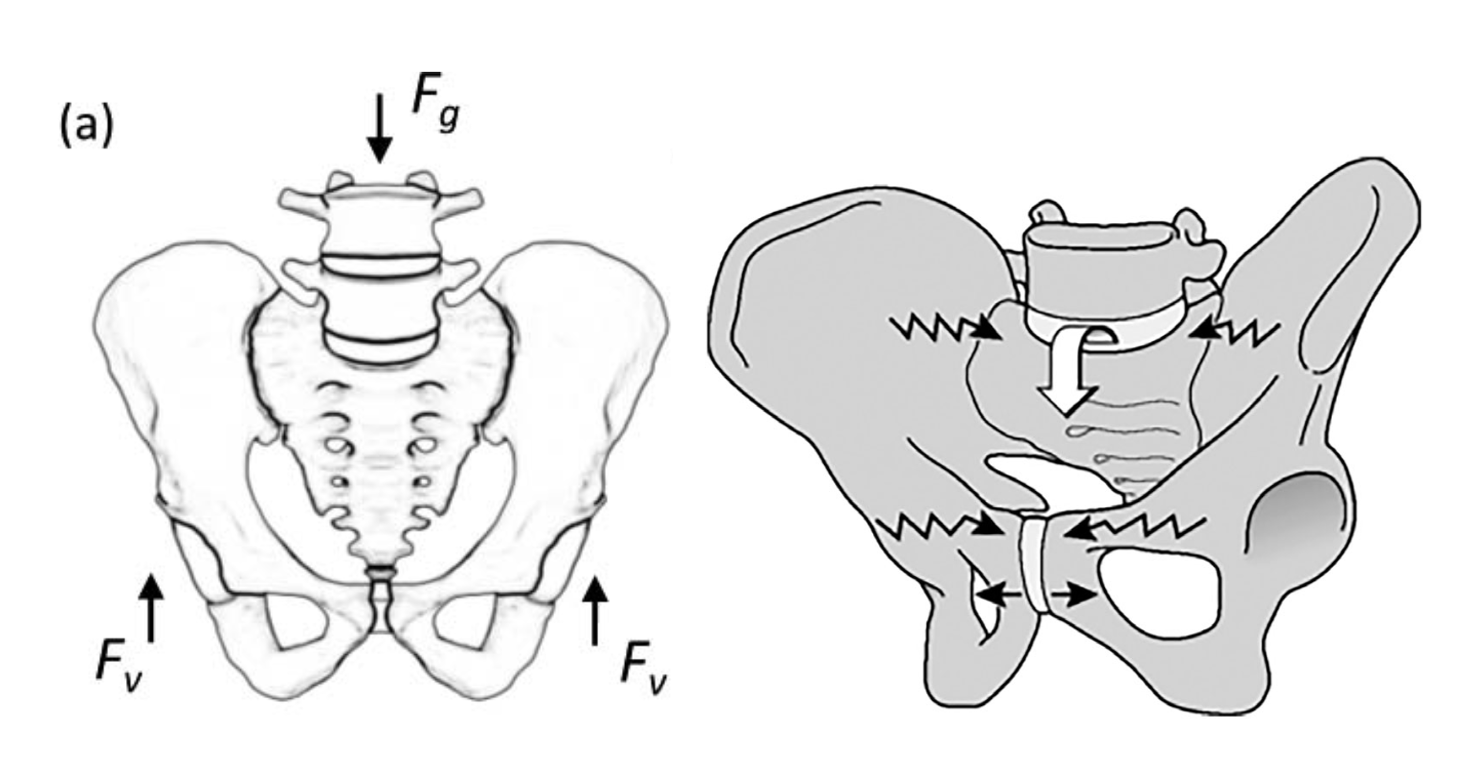
Fra Kiapour 2020 Fra Vleeming 2019
For belastningsrelaterte frakturer skiller en mellom stressfrakturer og insuffisiensfrakturer. Stressfrakturer er et resultat av for høy belastning på normalt bein over tid. Insuffiens fraktur oppstår ved normal belastning på et generelt svekket skjelett, for eksempel ved osteoporose eller osteopeni. Lav energitilgjengelighet kan over tid gi reduksjon i beinmineraltetthet og øke risikoen for fraktur.
En tredje type fraktur er patologiske frakturer. Disse oppstår som følge av et fokalt svekket skjelett, for eksempel ved en tumor eller metastaser.4
Dette dokumentet handler kun om stressreaksjoner/-frakturer i sacrum.
Klinisk presentasjon
Symptomene på stressfraktur i sacrum gir vanligvis belastningsrelaterte smerter i sete og lumbalcolumna. Smerteområdene kan imidlertid variere og inkludere smerte som radierer til sete, smerte i lyske. Symptomene kan også gi smerteutstråling til underekstremiteten, men det er sjeldent. Smertebildet varierer, og smerter fra ett av områdene kan dominere. Skadene kan derfor være vanskelig å oppdage. Sacrale stressfrakturer gir vanligvis ikke nevrologiske symptomer, men nerverot- irritasjon med tilhørende symptomer kan forekomme.3,9,10
Anamnese
I anamnesen må en kartlegge symptomer, oppstart, varighet, progresjon og variasjon, samt tidligere skader i samme område.
Det er viktig å innhente informasjon om underliggende indre og ytre faktorer som er forbundet med økt risiko for utvikling av stressfrakturer. Ytre faktorer inkluderer rask økning av treningsbelastning og endring av øvelsesutvalg. Indre faktorer omfatter blant annet lav energitilgjengelighet og eventuelle andre sykdommer/tilstander som kan medføre svekket benhelse. Indre og ytre faktorer virker ofte sammen i utviklingen av stressfrakturer i sacrum.11
Klinisk undersøkelse
De fleste pasientene har palpasjonsømhet over sacrum og IS-ledd, og nedsatt bevegelighet i lumbalcolumna. Det finnes imidlertid ingen klinisk test som har vist seg å ha høy spesifisitet for å påvise sacral stressfraktur.
Palpasjonsømhet mot sacrum ser ut til å være et av de viktigste funnene ved undersøkelsen. Fulcrum test i mageleie der undersøkeren gir trykk mot posteriore del av sacrum på høyre eller venstre side, kan være mer sensitiv enn ren palpasjon.
IS-leddstester kan være positive, men er ikke spesifikke for stressfrakturer i sacrum. Smerter ved hink, og positiv FABER test er også vanlige funn. 4,7,8,12
Differensial diagnoser inkluderer blant annet skivepatologi i nedre lumbal, trochanter bursitt, gluteal bursitt, bekken og intra-abdominale prosesser, spondyloarthropatier og spondylolisthese.3,7
Det kan være vanskelig å oppdage en stressfraktur i sacrum ved klinisk undersøkelse. Ved mistanke om stressfraktur bør pasienten henvises til MR.
MR utredning
MR er førstevalget ved mistanke om stressfraktur i sacrum. Frakturene produserer ikke kallus, og er derfor vanskelig å oppdage på røntgen.
De fleste pasienter med stressfraktur i sacrum presenterer symptomer som medfører henvisning til MR av LS- columna eller hofte. MR undersøkelse av LS-columna inkluderer vanligvis ikke hele sacrum. Ved valg av denne MR protokollen kan derfor skader i sacrum overses, spesielt dersom skaden er lokalisert til kaudale avsnitt av sacrum.
Protokoll for MR hofte inkluderer sacrum.
Dersom det kun henvises til målrettet undersøkelse av sacrum kan differensialdiagnoser i lumbal og hofte overses.
Dersom det er usikkert om hvor skaden sitter dekker en alle strukturer med MR av både LS-columna og hofte.
Det er pr i dag ikke utarbeidet MR klassifisering for stressfrakturer i sacrum.10
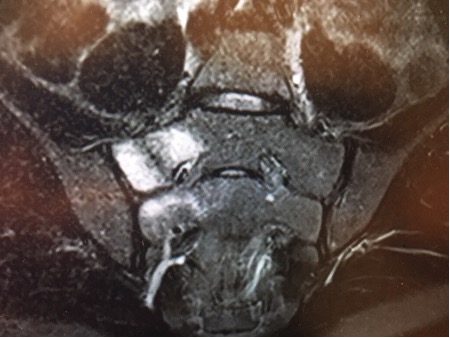
|
Akutt stressfraktur omgitt av margødem kranialt i høyre sacralvinge. Utbredelse mot 1. sacralforamen hvor det er ødem. |
MR henvisningen skal inneholde:
- Idrettsgren og nivå
- Symptomer; varighet og sideangivelse/lokalisasjon
- Eventuelt utstrålende smerter
- Traumemekanisme dersom traume
- Provoserende aktivitet eller bevegelse
- Hvor i fasen pasienten er; ute av idrett/i rehabilitering
- Kliniske differensialdiagnoser
-Tidligere skader og operasjoner i aktuelle område
Interne henvisningsrutiner
Ved mistanke om eller bekreftet stressreaksjon/-fraktur skal pasienten settes opp til lege med spesiell kompetanse innenfor området. Lege koordinerer videre utredning og rehabilitering, og kobler inn fysioterapeut, ernæringsfysiolog, psykiater, gynekolog, endokrinolog, ev andre spesialister etter behov.
Stipendutøvere utredes og følges opp i regi av OLT på alle områder etter behov. Utøvere på lavere nivåer må som regel henvises eksternt hvis det er behov for ernæringsfysiolog, psykolog etc, gjerne via forsikring/Idrettens helsesenter hvis utøver har dette.
Medisinsk utredning
Lege vurderer bredt og utreder mulige medvirkende bakenforliggende medisinske årsaker til stressfrakturen. Det finnes en rekke sykdommer, tilstander og medikamenter som kan gi sekundær osteopeni/osteoporose og svekket benhelse.
Det vanligste i utøverpopulasjonen vil være funn av REDS (Relative Energy Deficiency in Sport), det vil si lav energitilgjengelighet. REDS medfører et syndrom hvor blant annet lave kjønnshormonnivåer og redusert benhelse er fremtredende. Utøvere fra idretter der vekt er en prestasjonsvariabel rapporterer ofte perioder med restriktivt energiinntak, noe som kan utvikle seg til en kronisk lav energitilgjengelighet. Konsekvensene av lav energitilgjengelighet over tid er blant annet endringer i hormonprofil, primær eller sekundær amenoré for kvinner, redusert testosteronkonsentrasjon for menn og påfølgende tap av beinmasse. Utøvere med amenoré tenderer til å ha et svakt skjelett med dårlig mikroarkitektur og har dermed 2-4 ganger større risiko for stressfrakturer enn utøvere med normal menstruasjon. Foreløpige studier indikerer at mannlige utøvere med lav energitilgjengelighet har en lignende fysiologisk prosess.
Menstruasjonsforstyrrelse er til stede hos 75% av kvinnelige utøvere med stressfrakturer i trabekulært bein, men kun hos 12,5% hos utøvere med skader på kortikalt bein.13
Mange kvinnelige utøvere bruker prevensjon som påvirker blødning og menstruasjonssyklus. Spørsmål utlukkende om normal menstruasjon har derfor begrenset nytte. Endring av kropps- sammensetning og eventuell vektreduksjon bør klarlegges.
DEXA-måling brukes for å se på total og regional benmineraltetthet (BMD). Diagnostiske kriterier for osteopeni og osteoporose i en utøverpopulasjon er henholdsvis Z-score mellom -1,0 og -2,0 og Z-score ≤‑2,0 standardavvik sammenliknet med referansepopulasjonen, samt historikk på lav energitilgjengelighet, lavt østrogennivå for kvinner, stressfrakturer eller andre sekundære kliniske risikofaktorer for brudd. Idrettsutøvere har generelt høyere BMD sammenlignet med aldersbestemte referansepopulasjoner, grunnet flere år med stor belastning på skjelettet. DEXA gjøres ofte, for eksempel ved REDS eller ved treg tilheling eller gjentatte stressfrakturer. Bentetthetsmåling er vesentlig i vurderingen av benhelsen, men sier ikke alt, og det forskes på supplerende metoder for å kartlegge benkvalitet.
DEXA kan gi viktig prognostisk informasjon med hensyn til tid til retur til idrett. Bone mass index (BMI) forklarer mer enn 68% av variasjon i tid til retur til idrett. Dette gjelder spesielt for skader i trabekulært bein. Disse funnene gir indikasjon for videre undersøkelse med DEXA ved diagnostisering av stressreaksjon/fraktur.13
Også andre tilstander enn REDS bør vurderes ved mistanke om suboptimal benhelse. Malabsorpsjon i tarm kan medføre osteopeni/osteoporose. I følge NEL er det grunn til å anta at den reelle prevalensen av Cøliaki i Norge er på 0,5 -1 %. Kun 25-40 % får stilt diagnosen. Minst 20 % er asymptomatiske. Det er høyere forekomst hos de med førstegradsslektninger med cøliaki, samt ved andre autoimmune tilstander som diabetes og autoimmun tyroideasykdom.
Pasienter med ubehandlet cøliaki kan ha forstyrrelser i calciumstoffskiftet og har en økt forekomst av osteopeni og osteoporose. Hyppig ses en komorbiditet med D-vitamin mangel og/eller sekundær hyperparatyreoidisme. Ubehandlet cøliaki kan medføre malabsorpsjon av jern, folsyre, B12, kalsium og fettoppløslige vitaminer, også når det ikke foreligger diare (diare oppstår ofte først når distale deler av tynntarmen affiseres). Med andre ord bør terskelen være lav for å utrede for cøliaki hos disse utøverne.
Av andre tilstander som kan gi sekundær osteoporose/osteopeni, er det mest aktuelt å nevne endokrine sykdommer som hypertyreose og hyperparathyroidisme og revmatiske tilstander som Bekhterev.
Lege vil i hvert tilfelle vurdere hvilke blodprøver som skal tas, aktuelle prøver kan være:
Hb, Leukocytter m/diff, ferritin, TSH, T4, LH, FSH, østradiol/testosteron, SHBG, ALP, PTH, Ca, Fosfat, Mg, albumin, Vit D, Antitransglutaminase-antistoffer
Ernæring
Stressfrakturer som inkluderer trabekulært bein er tettere knyttet opp mot lavt energiinntak og spiseforstyrrelser enn stressfrakturer i utelukkende kortikalt bein. Kvinner med oligo-/amenorea har også større sannsynlighet for å utvikle stressreaksjon med høyere gradering. De har også lavere beinmasse ved DEXA undersøkelse. Lavere beinmasse kan være assosiert med utvikling av høyere grad av stressreaksjon og fraktur. I studien til Nattiv et al rapporterte 75% av kvinner med trabekulær beinskade uregelmessig menstruasjon, mot kun 12,5% av kvinner med kortikal skade. 13
Det er viktig å optimalisere ernæring under tilhelingsprosessen av stressfrakturer, uavhengig av BMD-status, og de viktigste faktorene er energitilgjengelighet, kalsium og vitamin D.
Ved påvist stressreaksjon/stressfraktur er det anbefalt et totalinntak av kalsium på 1500 mg/dag.
For stipendutøvere utfører ernæringsavdelingen en analyse av inntak gjennom kosten. For andre utøvere kan helsepersonell spørre direkte om inntak av meieriprodukter. De bør innta 3 porsjoner med meieriprodukter daglig for vedlikehold (for eksempel en yoghurt, en skive med ost som pålegg, ett glass melk). Utøveren kan videre supplementeres med 500 mg kalsium morgen og 500 mg kveld, i tråd med IOCs anbefalinger.14-16
Det er en utfordring med lave vitamin D-verdier i befolkningen generelt, noe som også gjenspeiles i idretten. Man ser en korrelasjon mellom for lavt kalsium og vitamin D-inntak/status hos løpere og forekomst av stressfrakturer.17 En blodprøve vil raskt vise D – vitamin status, og utøver bør supplementeres dersom resultatene viser 25(OH)d(konsentrasjon av vitamin D3 målt i blod) <75. Etter Olympiatoppens retningslinjer bør verdier <50 supplementers med 50-100ɥg vitamin D3 daglig. Verdier mellom 50-75 supplementeres med 40-60 ɥg/dag. Verdier >75 optimaliseres med vitamin D-inntak gjennom kosten, evt. supplementert med 10-20 ɥg/dag for vedlikehold.
Utøvere som er diagnostisert med spiseforstyrrelse har vist signifikant lenger tid før retur til idrett i forhold til friske utøvere etter stressfraktur.13
Retningslinjer for rehabilitering
Målet med rehabiliteringen er å få skaden til å tilhele. Belastningsstyring skjer på grunnlag av symptomer og tidslinje. Det må tas hensyn til energiforbruk ved REDs problematikk, og total treningsbelasting må monitoreres.
Fase 1:
Hovedmålet er å bli smertefri ved ADL. Pasienten kontrollerer all aktivitet basert på smerte. All aktivitet som involverer underekstremiteten skal være smertefri, det vil si 0 på en 0-10 smerteskala. Dersom pasienten har smerter ved normal gange skal det avlastes med krykker til han/hun kan gå uten smerter.
Pasienten kan trene i vann med svømming eller aquajogg dersom treningen er symptomfri.
Når pasienten kan gå normalt uten smerter seponeres krykkene. Dersom det skulle oppstå symptomer må pasienten over på krykkeavlastning igjen.
Overgang til fase 2 kan skje når pasienten har vært smertefri ved normal gange i 5 dager.
Fase 2:
Oppstart av lavbelastet aktivitet.
Aktuelle øvelser i fase 2:
Trening i vann
Ergometersykkel
Stake-ergometer
Gange på flat tredemølle.
All aktivitet skal være innenfor smertegrensen, det vil si 0 på en 0-10 smerteskala.
Etterhvert overgang til Alter-G mølle annenhver dag. Tidspunkt for overgang til Alter-G vil variere ut fra grad av skade. Oppstart på Alter-G mølle med 80% kroppsbelastning på flat mølle. Lav hastighet innledningsvis, 8-9km/t. Progresjonen med hensyn til kroppsbelastning og hastighet vil være individuell, men alltid strengt styrt innenfor smertegrensen,
Varighet av fase 2 vil også være individuell. Progresjon til fase 3 forutsetter at pasienten har vært symptomfri i all aktivitet, inkludert smertefri løping på Alter-G med 95% kroppsbelastning i 12 km/t.
Idrettsspesifikk styrketrening kan gjennomføres innenfor symptomgrensen. Det må da velges 2-beins øvelser for å unngå økt belastning på sacrum.
Fase 3:
Pasienten skal ha vært smertefri gjennom progresjonen i fase 2, samt vært smertefri ved all aktivitet, og ved kliniske tester før progresjon til fase 3.
Oppstart med idrettsspesifikk trening annenhver dag, med kontroll av symptomer, som skal være 0 på en 0-10 smerteskala.
Korte perioder med full belastning innen aktuelle idrett. Start med så lite som <5 min. Gradvis økende varighet.
Fase 4:
Overgang til ubegrenset idrettsaktivitet. I starten annenhver dag
En kan vurdere trenings-sykluser der en har 2 uker belastning og en uke med rolig belastning for å optimalisere i forhold til remodelleringsprosessen, etter Romani et al18. Hver treningssyklus består da av 2 uker ubegrenset belastning + 1 uke rolig belastning, som repeteres én gang.
Tid til retur til idrett
Det er gjort få studier som gir informasjon om tid til retur til idrett etter stressreaksjon/fraktur i sacrum. Det meste er basert på enkelt caser med ulik kvalitet. Tid til retur til idrett varierer mellom casestudier, og ligger hovedsakelig mellom 6 og 12 uker.19,20,21,22,23
Harris et al4 anbefaler alternativ trening i 6-8 uker i sin artikkel. Kahnov et al 19 anbefaler avlastning i 4-6 uker og deretter gradvis økning av belastende trening.
I en systematisk oversikt over stressfrakturer i underekstremiteten fant Nattiv et al13 at gjennomsnittlig tid til retur til idrett var betydelig lenger for høygradige skader i områder med mye trabekulært bein i forhold til kortikalt bein, henholdsvis median 38,1 (6,4) uker mot 18,6 (2,1) uker. For mindre alvorlige skader, grad 1 og 2, var det ikke signifikant forskjell i tid til retur til idrett. I materialet var det kun 3 sacrum frakturer.
Stressfrakturer i sacrum involverer trabekulært bein. Dette gir altså potensielt lenger tilhelingstid for de mer alvorligs skadene enn ved stressfrakturer i kortikalt bein.13
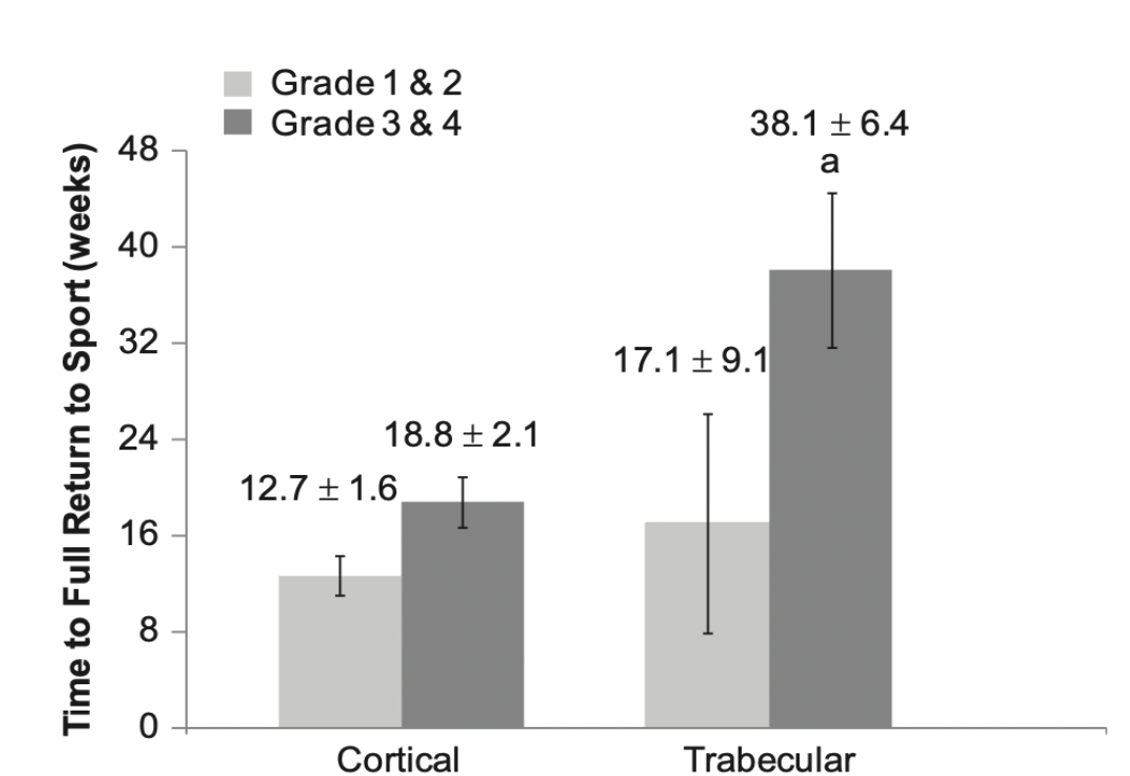
Fra Nattiv et al 2013
Olympiatoppen anbefaler alternativ trening i minimum 6-8 uker for lav-gradige stressreaksjoner, og minimum 14 uker for høygradige skader med frakturlinje. Her vil det være store individuelle variasjoner basert på grad av skade og øvrige risikofaktorer. Ellers følger rehabilitering av stressreaksjoner/frakturer i sacrum samme retningslinjer som for andre stressfrakturer med belastningsstyring innenfor smertegrensen, det vil si 0 på en 0-10 smerteskala.
Referanser:
1 Kiapour, A. et al. Biomechanics of the Sacroiliac Joint: Anatomy, Function, Biomechanics, Sexual Dimorphism, and Causes of Pain. Int J Spine Surg 14, 3-13, doi:10.14444/6077 (2020).
2 Vleeming, A. & Schuenke, M. Form and Force Closure of the Sacroiliac Joints. PM & R : the journal of injury, function, and rehabilitation 11 Suppl 1, S24-S31, doi:10.1002/pmrj.12205 (2019).
3 Yoder, K. et al. Risk factors associated with sacral stress fractures: a systematic review. The Journal of manual & manipulative therapy 23, 84-92, doi:10.1179/2042618613Y.0000000055 (2015).
4 Harris, C. E., 3rd, Vincent, H. K. & Vincent, K. R. Sacral Stress Fractures: They See You, But Are You Seeing Them? Curr Sports Med Rep 15, 73, doi:10.1249/JSR.0000000000000245 (2016).
5 Khoo, B. C. C., Goh, J. C. H. & Bose, K. A biomechanical model to determine lumbosacral loads during single stance phase in normal gait. Medical Engineering & Physics 17, 27-35, doi:https://doi.org/10.1016/1350-4533(95)90374-K (1995).
6 Linstrom, N. J. et al. Anatomical and biomechanical analyses of the unique and consistent locations of sacral insufficiency fractures. Spine 34, 309-315, doi:10.1097/BRS.0b013e318191ea01 (2009).
7 Zaman, F. M., Frey, M. & Slipman, C. W. Sacral stress fractures. Curr Sports Med Rep 5, 37-43 (2006).
8 Mangla, J., Young, J. L., Thomas, T. O. & Karaikovic, E. E. Sacral stress fractures in children. Am J Orthop (Belle Mead NJ) 38, 232-236 (2009).
9 Major, N. M. & Helms, C. A. Sacral stress fractures in long-distance runners. AJR. American journal of roentgenology 174, 727-729, doi:10.2214/ajr.174.3.1740727 (2000).
10 Longhino, V., Bonora, C. & Sansone, V. The management of sacral stress fractures: current concepts. Clin Cases Miner Bone Metab 8, 19-23 (2011).
11 Feldman, J. J., Bowman, E. N., Phillips, B. B. & Weinlein, J. C. Tibial Stress Fractures in Athletes. The Orthopedic clinics of North America 47, 733-741, doi:10.1016/j.ocl.2016.05.015 (2016).
12 Vajapey, S., Matic, G., Hartz, C. & Miller, T. L. Sacral Stress Fractures: A Rare but Curable Cause of Back Pain in Athletes. Sports health 11, 446-452, doi:10.1177/1941738119854763 (2019).
13 Nattiv, A. et al. Correlation of MRI grading of bone stress injuries with clinical risk factors and return to play: a 5-year prospective study in collegiate track and field athletes. Am J Sports Med 41, 1930-1941, doi:10.1177/0363546513490645 (2013).
14 Thein-Nissenbaum, J. & Hammer, E. Treatment strategies for the female athlete triad in the adolescent athlete: current perspectives. Open Access J Sports Med 8, 85-95, doi:10.2147/OAJSM.S100026 (2017).
15 Mountjoy, M. et al. The IOC consensus statement: beyond the Female Athlete Triad--Relative Energy Deficiency in Sport (RED-S). Br J Sports Med 48, 491-497, doi:10.1136/bjsports-2014-093502 (2014).
16 Ackerman, K. E., Skrinar, G. S., Medvedova, E., Misra, M. & Miller, K. K. Estradiol levels predict bone mineral density in male collegiate athletes: a pilot study. Clin Endocrinol (Oxf) 76, 339-345, doi:10.1111/j.1365-2265.2011.04212.x (2012).
17 Giffin, K. L., Knight, K. B., Bass, M. A. & Valliant, M. W. Predisposing Risk Factors and Stress Fractures in Division I Cross Country Runners. J Strength Cond Res, doi:10.1519/jsc.0000000000002408 (2017).
18 Romani, W. A., Gieck, J. H., Perrin, D. H., Saliba, E. N. & Kahler, D. M. Mechanisms and management of stress fractures in physically active persons. Journal of athletic training 37, 306-314 (2002).
19 Kahanov, L., Eberman, L., Alvey, T., True, J. & Yeargin, B. Sacral stress fracture in a distance runner. J Am Osteopath Assoc 111, 585-591 (2011).
20 Silva, R. T., De Bortoli, A., Laurino, C. F., Abdalla, R. J. & Cohen, M. Sacral stress fracture: an unusual cause of low back pain in an amateur tennis player. Br J Sports Med 40, 460-461, doi:10.1136/bjsm.2005.023473 (2006).
21 Slipman, C. W., Gilchrist, R. V., Isaac, Z., Lenrow, D. A. & Chou, L. H. Sacral stress fracture in a female field hockey player. American journal of physical medicine & rehabilitation / Association of Academic Physiatrists 82, 893-896, doi:10.1097/01.PHM.0000091987.99243.5D (2003).
22 Takahashi, Y. et al. Sacral stress fracture in an amateur rugby player: a case report. J Med Case Rep 10, 327, doi:10.1186/s13256-016-1120-3 (2016).
23 Yuasa, Y. et al. Sacral Stress Fracture in an Amateur Badminton Player. Case Rep Orthop 2017, 4268981, doi:10.1155/2017/4268981 (2017).