Stress frakturer i tibia
Erik Iversen, Arne Larmo, Ellen Moen og Ina Garthe
Tibia er den vanligste lokalisasjon for stressfraktur/stressreaksjon i bein hos idrettsutøvere. Løpere er mest utsatt, spesielt langdistanseløpere. Mellom 33% og 75% av alle stressfrakturer oppstår i tibia for denne gruppen.1,2 Stressfrakturer oppstår som oftest i forbindelse med endret, eller økt, belastning,3 og oppstår i 3 områder i tibia; posteromediale korteks, anterolaterale korteks og tibiaplatået. Skader på posteromediale korteks er den vanligst, og hoveddelen av dette dokumentet omhandler disse skadene. Stressfrakturer i anteriore korteks, og tibiaplatået er relativ uvanlig sammenlignet med stressfrakturer i posteromediale korteks.
Stressfrakturer deles inn i høy- og lavrisiko basert på anatomisk lokalisasjon. Lav risiko frakturer har god prognose når de behandles med aktivitetsrestriksjon. Høyrisiko frakturer har større sjanse for forsinket tilheling eller non-union, spesielt dersom det tar litt til før diagnosen blir stilt. De tar vanligvis vesentlig lenger tid å tilhele enn lavrisiko skader. Skader på posteromediale korteks er en lavrisiko skade, mens skader på anterolaterale korteks og mediale malleol er høyrisiko skader.4
Stressfrakturer er et resultat av for høy belastning på normalt bein over tid.
Insuffisiensfrakturer oppstår ved normalt stress av generelt svekket bein. Insuffiens fraktur oppstår ved normal belastning på et generelt svekket skjelett, for eksempel ved osteoporose eller osteopeni. Lav energitilgjengelighet kan over tid gi reduksjon i beinmineraltetthet.
Patologiske frakturer betegner gjerne fraktur i et mer fokalt svekket skjelett, for eksempel ved en tumor. Insuffiens - og patologiske frakturer bør alltid være med i vurderingen ved skjelettaffeksjon.5
Utvikling av stressfrakturer
I følge Wolff’s lov vil en ytre mekanisk belastning gjøre at bein tilpasser seg belastningen den utsettes for over tid. Bein tilpasser seg belastning ved å endre både den indre trabekulære strukturen, og i den ytre kortikale overflaten av beinet, avhengig av beinets geometri og kreftene som virker på det. De lange knoklene, som for eksempel tibia, fungerer som en søyle og får mye av styrken sin fra kortikalt bein. Ved bøyning oppstår det kompresjonskrefter i korteks på en side, og traksjonskrefter på motsatt side, mens belastningen avtar til 0 mot midten av søylen. Som følge av dette skjer det meste av remodelleringen i tibia i korteks.6
Under løping utsettes tibia for kontaktkraft, ground reaction force (GRF), fra underlaget. Det er gjort en rekke studier på aksial kraft og hvor mye et bein tåler før det skades. Kortikalt bein hos mennesker kan tåle 4-10 millioner belastningssykluser med kompresjon før det oppstår skade.7 Dette er belastningsnivåer som ikke er enkle å nå, selv for profesjonelle utøvere.
Det totale stresset på et belastet bein kommer fra en kombinasjon av kontaktkreften mot bakken og bøyningskrefter fra muskeldrag. I følge Pauwels’ Theorem vil ytre krefter bøye beinet i en retning, mens kraften fra muskulatur vil bøye beinet i motsatt retning. Under løping vil summen av kreftene tenderer til å bøye tibia i en konkav posterio-medial retning.
Dette gir kompresjon av korteks postero-medialt, og tensjon antero-lateralt. Kompresjons-kraften kommer på toppen av bøyningsstresset. Den øker kompresjonen på den komprimerte overflaten ytterligere, og reduserer tensjonsstresset på motsatt side. Kreftene som tibia utsettes for gjenspeiles derfor ikke av GRF alene. Under løping er GRF 2-3 ganger kroppsvekt, mens distale del av tibia utsettes for krefter 6-14 ganger kroppsvekt på grunn av muskeldrag fra leggmuskulaturen. Belastingen på tibia er relativt lav i det foten treffer bakken, men øker i standfasen av løpssteget.8,9
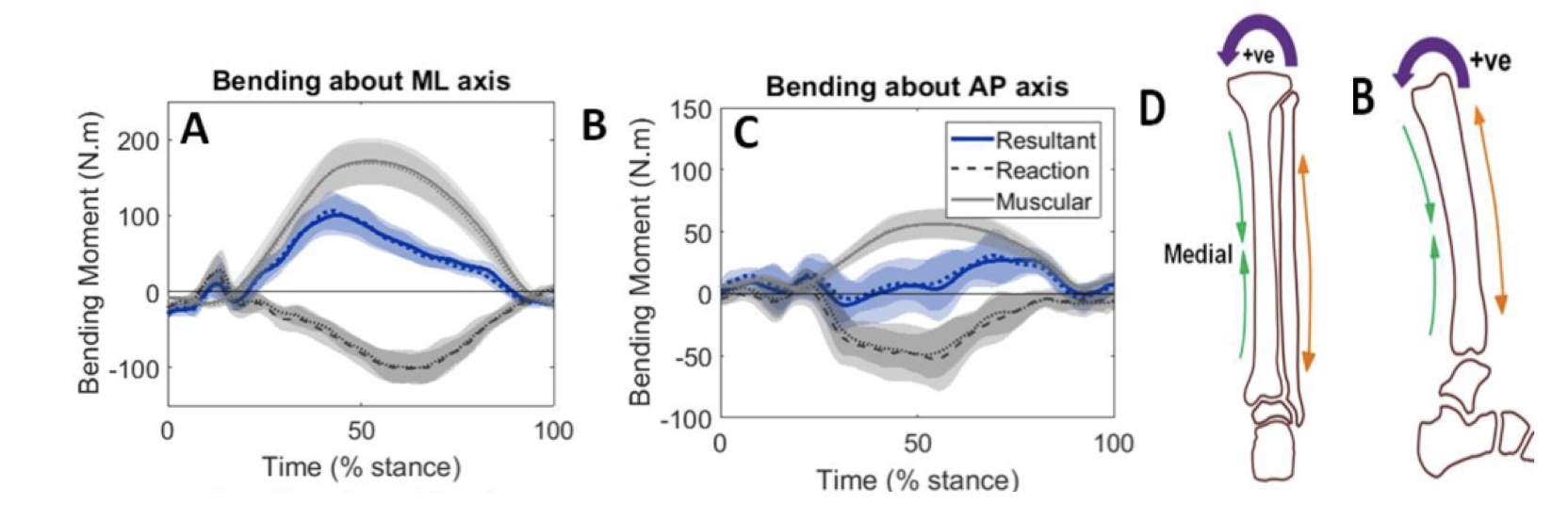
|
Fra Rice et al 2019 |
Stressfrakturer er ikke forårsaket av en spesifikk hendelse, men oppstår ved gjentatte eller økte belastninger over tid med for lite hvile. Aktiviteter som løping og hopping er normalt langt unna beinets grense for makroskopisk skade, men repetert belastning kan resultere i akkumulering av mikroskade på beinet. Mikroskader observeres som mikrosprekker, og er en naturlig konsekvens av belastning av friskt bein. For å reparere disse mikroskadene startes remodelleringsprosessen. Ved fortsatt belastning vil det kunne oppstå en situasjon med økende mikroskade som kan utvikle seg til en stressfraktur. Tidlig akkumulering av mikroskade med beinmargsødem kalles en stressreaksjon. Når det er synlig frakturlinje på MR, CT eller røntgenundersøkelse defineres skaden som en stressfraktur.10,7
Det er stor variasjon mellom utøvere og individuell belastning på tibia. Belastning på tibia er imidlertid sterkt korrelert med løpshastighet, og stigning.8,11 Det er også vist økende beinstress ved økende varighet av trening. Det er foreløpig ukjent hvor tidlig dette inntreffer. Det er vist en økning på 12-15% av maksimalt anteriort og posteriort stress ved løping i 20 minutter. Dette oppsto hos 12 av 14 testpersoner ved løping i moderat fart på tredemølle.9
Årsakssammenhengene for utvikling av stressfraktur er fortsatt ikke fullstendig klarlagt, og er sannsynligvis multifaktoriell. Histologiske undersøkelser med beinbiopsier har funnet at tidlig avbrudd av repetitivt stress hindrer progresjon mot en mer alvorlig fraktur.12
Remodellering
En komplett traumatisk fraktur tilheler ved dannelse av kallus som starter som brusk som videre går gjennom stadier av ossifikasjon. Først etter denne første stabiliseringsprosessen starter remodellering av beinet med rekonstruksjon av den lamellære beinstrukturen.
Tilheling av en stressfraktur går direkte, og kun, via remodellering.
Belastninger i idrettsaktivitet er vanligvis langt unna beinets grense for makroskopisk skade, men repetert belastning kan resultere i akkumulering av mikroskade på beinet. Mikroskader observeres som mikrosprekker og er en naturlig konsekvens av belastning av friskt bein. For å reparere disse mikroskadene startes remodelleringsprosessen.
Remodellering skjer ved at et team av ulike celler som kalles basic multicellular unit (BMU) resorberer og legger til nytt bein. Den følger alltid en fast sekvens med aktivering -> resorpsjon -> reversering -> formasjon.
Denne prosessen er normalt tett koblet, slik at totalt beinvolum og struktur forblir uendret. Dette sørger for strukturell integritet, samtidig som prosessen tillater at opp til 10 % av skjelettet byttes ut hvert år. Hele remodelleringsprosessen tar 120 – 200 dager for henholdsvis trabekulært og kortikalt bein.13
I første rekke i BMU’en kommer osteoklaster som, når de blir aktivert, starter å resorbere bein. I kortikalt bein lager osteoklastene 3-10 mm dype longitudinelle kanaler i beinet. Denne prosessen tar ca. 2 uker. Deretter starter en reverseringsfase som enda ikke er fullt kjent. Først blir den overflaten klargjort for deponering av ny bein matrix, og det skjer videre signalisering mellom celler som kobler resorpsjon til formasjon av bein. Prepareringen av beinoverflaten gjøres av osteoblast-lignende celler som fjerner umineralisert kollagen matrix og legger ned ikke-kollagen mineralisert matrix. Denne prosessen tar 4-5 uker.
Til slutt kommer rekker av osteoblaster som binder seg til reverseringssonen. Osteoblastene skiller ut type 1 kollagenrik osteoid matrix som videre blir mineralisert. Noen osteoblaster blir værende i denne matrixen, og blir omdannet til osteocytter. Denne prosessen tar ca. 4 måneder.13,6
Dersom belastningen opprettholdes kan det føre til videre resorpsjon og akselerert nedbrytning av korteks. Dette kan over tid utvikle seg til en stressreaksjon og videre mot en stressfraktur.
Symptomer
Pasienten opplever som oftest gradvis innsettende smerter, uten forutgående traume. Smerten øker ved vektbærende aktivitet. I startfasen øker smerten vanligvis mot slutten av øktene og avtar ved hvile. Ved fortsatt belastning vil symptomene øke gradvis og kan da vare utover aktivitet, og i ADL. Smerten kan da også være til stede om natten.14 Ved skader på posterolaterale og anteromediale korteks er skadeområdene er lett tilgjengelig for palpasjon. Ved stressreaksjon/fraktur er smertefokus som oftest i et begrenset område ~ 5 cm.
Stressfrakturer på tibiaplatået oppstår medialt og posteriort. Skaden kan lett feil-diagnostiseres da smertelokalisasjon, og palpasjonsømhet, er lik det en finner ved medial meniskskade, MCL, PFS, og pes anserinus bursitt. Pasientene rapporterer typisk gradvis innsettende smerte ved mediale proksimale del av tibia, uten forutgående traume. Det er vanligvis ikke innskrenket bevegelighet i kneleddet, eller økt væske i leddet. En bør derfor være oppmerksom på denne differensialdiagnosen hos løpere med medial knesmerte.15
Anamnese
Kartlegge symptomer, oppstart, varighet, progresjon og variasjon, samt tidligere skader i samme område.
Det er viktig å innhente informasjon om underliggende indre og ytre faktorer som er forbundet med risiko for utvikling av stressfrakturer. Ytre faktorer inkluderer rask økning av treningsbelastning, og endring av øvelsesutvalg. Indre faktorer omfatter blant annet lavenergitilgjengelighet og eventuelle andre sykdommer/ tilstander som kan medføre svekket benhelse. Indre og ytre faktorer henger ofte sammen i utvikling av stressfrakturer, for eksempel økt trening i kombinasjon med lavt energiinntak.14
Klinisk undersøkelse
Palpasjon av tibia
Belastningstester:
Hæl-dropp
Vristhopp
Hinketest
Fulcrum test – bøyningsmoment mot kanten av benken eller mot undersøkerens kne eller arm, reproduserer symptomene.
Observere evt hevelse og hudforandringer.
Utelukke skade på andre områder som kan gi symptomer i aktuelle område.
Vurdere risikofaktorer; Strukturelle avvik og lav muskelmasse, spesielt i leggen, kan øke risiko for økt stress på tibia.14
Se etter tegn på lav energitilgjengelighet eller spiseforstyrrelse som lite underhudsfett, økt behåring, blek hud, lite glans i hud / hår, dårlig tannstatus (NB. oppkast), lav puls/ BT.
Differensialdiagnoser
Kompartmentsyndrom har andre symptomer enn stressfraktur. Pasienten opplever ofte krampefølelse, brennende smerter eller trykksmerter i leggen som raskt bedres etter belastning. I tillegg til smerter under trening, kan pasienten også oppleve parestesier og/ eller kald fot på grunn av komprimerte nerver / blodtilførsel.16
Andre aktuelle tilstander er strekk/partielle rupturer, kontusjonsskader og DOMS.
Vær oppmerksom på røde flagg på alvorlig patologi; smerte uten mekanisk belastning, nattsmerter, feber/nedsatt allmenntilstand, vekttap, tidligere historie med cancer. Smerte uten fraktur kan være forårsaket av osteoid osteom eller annen beintumor. Mulig infeksjon, i hud/ bløtdeler eller i bein (osteomyelitt) bør vurderes, spesielt hos barn og unge.
Medialt tibialt smertesyndrom (MTSS), eller traksjonsperiostitt, sees på som en tidlig fase i et kontinuum i utviklingen via stressreaksjon, til stressfraktur. Denne tilstanden normaliseres vanligvis ved avlastning i en kortere periode.
Det kan være utfordrende å skille denne tilstanden fra tibial stressfraktur, men diagnosen kan med stor sikkerhet stilles ut fra anamnese og klinisk undersøkelse. MR har ikke vist økt prediktiv verdi for prognose med hensyn til tid til retur til idrett.16
Klinisk er distale 2/3 av tibia palpasjonsømt over et større område langs posteromediale kant av tibia. Ved MTSS er det vanligvis palpasjonssmerte i et område lenger enn 5cm. Smerter i et mer avgrenset område øker mistanken mot stressreaksjon/fraktur. Dersom det ikke er tegn på andre tilstander kan en med stor sikkerhet stille diagnosen MTSS. Dersom konservativ behandling ikke gir symptomlette, eller det er usikkerhet rundt diagnosen, bør pasienten henvises til MR. Økt pronasjon øker risikoen for MTSS.14
MR
Det er viktig å diagnostisere stressreaksjoner i så tidlig stadie som mulig for å hindre videre utvikling og lenger tilhelingstid. MR kan plukke opp stressreaksjoner før det oppstår en fraktur. Fredericsons klassifikasjon er korrelert både med kliniske symptomer og tid til retur til idrett for skader i tibia. Periostealt ødem er ikke alltid til stede, og er ikke et nødvendig kriterium for diagnosen beinstress.12
MR er vanligvis førstevalg ved mistanke om stressfraktur. MR har en sensitivitet på 82% og spesifisitet på 100% for å detektere beinstress. Det finnes en rekke klassifiseringssystemer, men vi bruker Fredericsons klassifikasjonssystem for stressreaksjon/fraktur i tibia.
Grad 1 = kun periostealt ødem
Grad 2 = beinmargsødem på T2 vektede MR bilder (Stressreaksjon)
Grad 3 = beinmargsødem på både T1 og T2 vektede MR bilder (Stressreaksjon)
Grad 4a = multiple fokale områder med intrakortikale signalforandringer (Stressreaksjon)
Grad 4b = lineære områder med intrakortikale signalforandringer (Stressfraktur)
MR er svært sensitivt for beinmargsødem, men har dårligere forutsetninger for å påvise resorpsjon av bein. En stressreaksjon starter alltid med resorpsjon av bein. Ved fortsatt belastning vil resorpsjonen dominere, og ostekastene rekker ikke å legge ned nytt bein i samme tempo. Ved funn av beinmargsødem kan en derfor forvente at den fysiologiske prosessen har kommet lenger enn det MR påviser. Det betyr at selv ved lavere gradering der det kun er beinmargsødem på MR, vil man trenge en lengre periode med redusert belastning. MR viser heller ikke mekanisk styrke i beinet
MR henvisningen skal inneholde:
- Idrettsgren og nivå
- Symptomer og sideangivelse/lokalisasjon av symptomer
- Evt utstrålende smerter
- Varighet, og traumemekanisme dersom traume
- Provoserende aktivitet eller bevegelse
- Hvor i fasen er vi – ute av idrett/ i rehabilitering
- Differensialdiagnoser klinisk
-Tidligere skader og operasjoner i aktuelle område
Klinisk relevans
Symptomer samsvarer dårlig med alvorlighetsgrad basert på MR. Det er imidlertid vist en trend for høyere MR klassifisering (grad 1-4) og retur til idrett. Jo høyere gradering, jo lenger tid til tilheling. 17,12,18,19,20 Tid til retur til idrett varierer imidlertid mellom studiene, og det er ikke alltid statistisk signifikans korrelasjon mellom MR gradering og tid til retur til idrett.
Det er imidlertid signifikant forskjell i for tid til retur til idrett mellom skader i høyrisiko-områder sammenlignet med lavrisiko-områder.21
Det er ulik tilnærming til MR gradering og tid til retur til idrett blant ulike forfattere. Noen velger å dele skadene inn i stressreaksjon (grad 1 og 2 Fredericson) og stressfraktur (grad 3 og 4 Fredericson), evt i kombinasjon med om det er en høy- eller lavrisiko skade. Andre baserer tidslinje på de ulike graderingene, og spesifiserer tid til retur til idrett ut fra disse.
Jamieson et al19 brukte Kaeding-miller klassifikasjon for å gradere stressfrakturer i tibia hos en gruppe friidrettsutøvere. Denne klassifiseringen er forskjellig fra Fredericsons. Grad 1 og 2 indikerer stressreaksjon uten frakturlinje, mens grad 3-5 indikerer stressfraktur med økende alvorlighetsgrad.
Gjennomsnittlig tid til retur til idrett:
Grad 2 (stressreaksjon): 11,7 uker (5-27 uker)
Grad 3 (stressfraktur) 12,4 uker (10-18 uker).
Grad 5 (stressfraktur) 17 uker (kun 2 pasienter).
Selv om forholdet mellom tid til retur til idrett og MR klassifisering ikke nådde statistisk signifikans var det en positiv korrelasjon mellom variablene som indikerer at høyere MR gradering gir lengre rehabiliteringstid.
Dobrindt et al21 brukte også en forenklet gradering der de kombinerte grad 1 og 2 som lavgradig stressfraktur/reaksjon, og 3-4 som høygradig stressreaksjon. I tillegg ble skadene vurdert som lav- eller høyrisiko basert på anatomisk lokalisasjon. Dersom stressfrakturen er enten høygradig (grad 3 og 4) og/eller er lokalisert til et høyrisikoområde kan en forvente lang rehabiliteringstid. Forfatterne fant følgende tid til retur til idrett:
Lav risiko lokalisasjon og lav gradering (1-2) 61 dager, median 50 dager.
Lav risiko lokalisasjon og høy gradering (3-4) 153 dager, median 86 dager.
Høy risiko lokalisasjon og lav gradering (1-2) 135 dager, median 70 dager.
Høy risiko lokalisasjon og høy gradering (3-4) 131 dager, median 89 dager.
I en systematisk review fra Nattiv et al12 fant de følgende gjennomsnittlige tid før retur til idrett.
Grad 1: 11,4 (± 4,5) uker
Grad 2: 13,5 (± 2,1) uker
Grad 3: 18,8 (± 2,9) uker
Grad 4: 31,7 (± 3,6) uker
Arendt et al20 demonstrerte en signifikant korrelasjon mellom MR grad og retur til idrett. Høyere gradering (grad 3 og 4) ga lengre tid til retur til idrett enn lavere gradering.
Gjennomsnittlig retur til idrett:
Grad 1: 3,3 uker
Grad 2: 5,5 uker
Grad 3: 11,4 uker
Grad 4: 14,3 uker
Kijowski et al22 fant følgende tid til retur til idrett:
Grad 1: 3–20 dager, median 20 dager, mean 15.6 dager (SD 9.2)
Grad 2: 14–65 dager, median 43 dager, mean dager 39.4 (SD 12.8)
Grad 3: 18–90 dager, median 46 dager, mean 48.4 dager (SD 19.7)
Grad 4a: 40–50 dager, median 42 mean 43.5 (SD 4.4)
Grad 4b: 30–157 dager, median 64 mean 70.6 (SD 33.2)
De fant ikke signifikant forskjell mellom grad 2, 3 og 4a med hensyn til periostealt- eller beinmargsødem, eller tid til retur til idrett. Grad 1 har kortere, og grad 4b har signifikant lenger tid til retur til idrett enn grad 2, 3 og 4a. De argumenterer derfor for at Fredericson grad 2, 3 og 4a klinisk kan kombineres til en kategori.22
Det er vist reduksjon av MR gradering (Fredericson) fra 3,2 til 0,8, og reduksjon i størrelse på beinmargsødem fra 5,0cm til 0,9cm etter 12 ukers avlastning.23
I en studie av 21 langdistanseløpere hadde 43% asymptomatiske stressreaksjoner i tibia. Det var 4 grad 1 skader, 8 grad 2 skader, og 2 grad 3 skader. Ingen av løperne med asymptomatisk beinstress på MR utviklet symptomer på stressfraktur i løpet av oppfølgingsperioden (7 ble fulgt i 48 måneder, og 2 i 12 måneder. Det ble gjort ukentlig skaderapportering i denne perioden. Funn forenlig med stressreaksjon på MR, uten kliniske symptomer, var ikke relatert til videre utvikling av stressreaksjon/fraktur ved fortsatt belastning. Funnene representerer sannsynligvis den høye belastningen som langdistanseløpere utsettes for.24 I en studie med pasienter som var diagnostisert med stressfraktur (grad 3 og 4) hadde flesteparten (11 av 14) smerter ved normal gange, og alle hadde smerter ved løping.25
I en studie av militært personell ble pasienter med grad 1 og 2 stressreaksjoner overført til aktiv tjeneste uten avlastning. Av 14 pasienter utviklet 6 av dem høyere gradering, mens 8 gikk tilbake til normale funn. Stressfrakturer kan altså gå tilbake selv ved belastning ved lavere graderinger, men stresset på beinet bør reduseres for at ikke noen skal utvikle skaden videre.26 Det er viktig å holde belastningene under symptomgrensen.20
Tidlig deteksjon av skaden er viktig for å hindre utvikling mot høyere MR gradering og lengre rehabiliteringstid. Det er stor variasjon i tid til retur til idrett blant pasienter med samme gradering, men rehabiliteringstid øker ved økende gradering. MR klassifiseringen vil dermed kun bli retningsgivende i forhold til tid til retur til idrett. Noen pasienter vil være i stand til å returnere til idrett tidligere enn andre. Symptomstyring i rehabiliteringsfasen er essensielt. Det er viktig å holde symptomene på 0 vurdert på en 0-10 smerteskala.
Tid til retur til idrett varierer mellom pasienter, og kan kun brukes som en rettledning for forventet rehabiliteringstid for pasienten. Se avsnitt om behandling for veiledende tid til retur til idrett basert på aktuelle studier.
Interne henvisningsrutiner
Ved mistanke om eller bekreftet stressreaksjon/-fraktur skal pasienten settes opp til lege med kompetanse og interesse innenfor området. Lege koordinerer videre utredning og rehabilitering, og kobler inn fysioterapeut, ernæringsfysiolog, psykiater, gynekolog, endokrinolog, ev andre spesialister etter behov.
Stipend utøvere utredes og følges opp i regi av OLT på alle områder etter behov. Utøvere på lavere nivåer må som regel henvises eksternt hvis behov til ernæringsfysiolog, psykolog etc, gjerne via forsikring/ Idrettens helsesenter hvis utøver har dette.
Medisinsk utredning
Lege vurderer bredt og utreder mulige medvirkende bakenforliggende medisinske årsaker til stressfrakturen. Det finnes en rekke sykdommer, tilstander og medikamenter som kan gi sekundær osteopeni/ osteoporose og svekket benhelse.
Det vanligste i utøverpopulasjonen vil være funn av REDS (Relative Energy Deficiency in Sport), dvs lav energitilgjengelighet. REDS medfører et syndrom hvor blant annet lave kjønnshormonnivåer og redusert benhelse er fremtredende. Utøvere fra idretter der vekt er en prestasjonsvariabel rapporterer ofte perioder med restriktivt energiinntak, noe som kan utvikle seg til en kronisk lav energitilgjengelighet. Konsekvensene av lav energitilgjengelighet over tid er blant annet endringer i hormonprofil, primær eller sekundær amenoré for kvinner, redusert testosteronkonsentrasjon for menn og påfølgende tap av beinmasse. Utøvere med amenoré tenderer til å ha et svakt skjelett med dårlig mikroarkitektur og har dermed 2-4 ganger større risiko for stressfrakturer enn utøvere med normal menstruasjon. Foreløpige studier indikerer at mannlige utøvere med lav energitilgjengelighet har en lignende fysiologisk prosess.
Menstruasjonsforstyrrelse er til stede hos 75% av kvinnelige utøvere med stressfrakturer i trabekulært bein, men kun hos 12,5% hos utøvere med skader på kortikalt bein.12
Mange kvinnelige utøvere bruker prevensjon som påvirker blødning og menstruasjonssyklus. Spørsmål utlukkende om normal menstruasjon har derfor begrenset nytte. Endring av kropps sammensetning og eventuell vektreduksjon bør klarlegges.
DEXA-måling brukes for å se på total og regional benmineraltetthet (BMD). Diagnostiske kriterier for osteopeni og osteoporose i en utøverpopulasjon er henholdsvis Z-score mellom -1,0 og -2,0 og Z-score ≤‑2,0 standardavvik sammenliknet med referansepopulasjonen, samt historikk på lav energitilgjengelighet, lavt østrogennivå for kvinner, stressfrakturer eller andre sekundære kliniske risikofaktorer for brudd. Idrettsutøvere har generelt høyere BMD sammenlignet med aldersbestemte referansepopulasjoner, grunnet flere år med stor belastning på skjelettet. DEXA gjøres ofte, for eksempel ved REDS eller ved treg tilheling eller gjentatte stressfrakturer.. Bentetthetsmåling er vesentlig i vurderingen av benhelsen, men sier ikke alt, og det forskes på supplerende metoder for å kartlegge benkvalitet.
DEXA kan gi viktig prognostisk informasjon med hensyn tid til retur til idrett. Bone mass index (BMI) forklarer mer enn 68% av variasjon i tid til retur til idrett. Dette gjelder spesielt for skader i trabekulært bein. Disse funnene gir indikasjon for videre undersøkelse med DEXA ved diagnostisering av stressreaksjon/fraktur.12
Også andre tilstander enn REDS bør vurderes ved mistanke om suboptimal benhelse. Malabsorpsjon i tarm kan medføre osteopeni/ osteoporose. I følge NEL er det grunn til å anta at den reelle prevalensen av Cøliaki i Norge er på 0,5 -1 %. Kun 25-40 % får stilt diagnosen. Minst 20 % er asymptomatiske. Det er høyere forekomst hos de med førstegradsslektninger med cøliaki, samt ved andre autoimmune tilstander som diabetes og autoimmun tyroideasykdom.
Pasienter med ubehandlet cøliaki kan ha forstyrrelser i calciumstoffskiftet og har en økt forekomst av osteopeni og osteoporose. Hyppig ses en komorbiditet med D-vitamin mangel og/ eller sekundær hyperparatyreoidisme. Ubehandlet cøliaki kan medføre malabsorpsjon av jern, folsyre, B12, kalsium og fettoppløslige vitaminer, også når det ikke foreligger diare (diare oppstår ofte først når distale deler av tynntarmen affiseres). Med andre ord bør terskelen være lav for å utrede for cøliaki hos disse utøverne.
Av andre tilstander som kan gi sekundær osteoporose/ osteopeni, er det mest aktuelt å nevne endokrine sykdommer som hypertyreose og hyperparathyroidisme, og revmatiske tilstander som Bekhterev.
Lege vil i hvert tilfelle vurdere hvilke blodprøver som skal tas, aktuelle prøver kan være:
Hb, Leukocytter m/diff, ferritin, TSH, T4, LH, FSH, østradiol/ testosteron, SHBG, ALP, PTH, Ca, Fosfat, Mg, albumin, Vit D, Antitransglutaminase- antistoffer.
Medisinsk behandling
Østrogenplaster
Vurderes for å ivareta benhelsen hos utøvere med vedvarende amenore. Utøver må være under god oppfølging mht ernæring parallelt. I regi av gynekolog Åsle Marit Ullern.
Aclasta (bisfosfonat),
Kan vurderes ved stressfraktur som ikke tilheler med normal avlastningstid eller ved 2. gangs (eller mer) stressfraktur. I regi av endokrinolog Erik Fink Eriksen.
NSAIDS
Data fra dyrestudier, og et begrenset antall studier på mennesker, indikerer at NSAIDS (COX2-hemmere) bør ansees som en potensiell risikofaktor for forsinket frakturtilhelning. Pasienter som har påvist stressfraktur bør derfor ikke bruke NSAIDS.27 Dette gjelder også tidlig i behandlingsforløpet.28
Ernæring
Det er viktig å optimalisere ernæring under tilhelingsprosessen av stressfrakturer, uavhengig av BMD-status, og de viktigste faktorene er energitilgjengelighet, kalsium og vitamin D.
Ved påvist stressreaksjon/ stressfraktur er det anbefalt et totalinntak av kalsium på 1500 mg/dag.
For stipendutøvere utfører ernæringsavdelingen en analyse av inntak gjennom kosten. For andre utøvere kan helsepersonell spørre direkte om inntak av meieriprodukter. Alle bør innta minst 3 porsjoner med meieriprodukter daglig for vedlikehold (for eksempel en yoghurt, en skive med ost som pålegg, ett glass melk). Utøvere med stressfraktur kan videre supplementeres med 500 mg kalsium morgen og 500 mg kveld, i tråd med IOCs anbefalinger.29-31
Det er en utfordring med lave vitamin D-verdier i befolkningen generelt, noe som også gjenspeiles i idretten. Man ser en korrelasjon mellom for lavt kalsium og vitamin D-inntak/status hos løpere og forekomst av stressfrakturer.32 En blodprøve vil raskt vise D – vitamin status og utøver bør supplementeres dersom resultatene viser 25(OH)d( konsentrasjon av vitamin D3 målt i blod) <75. Etter Olympiatoppens retningslinjer bør verdier <50 supplementers med 50-100ug vitamin D3 daglig. Verdier mellom 50-75 supplementeres med 40-60 ug/dag. Verdier >75 optimaliseres med vitamin D-inntak gjennom kosten, evt. supplementert med 10-20 ug/dag for vedlikehold.
Utøvere som er diagnostisert med spiseforstyrrelse har vist signifikant lenger tid før retur til idrett i forhold til friske utøvere (31.3 ± 4.3 vs 15.4 ± 1.7 uker). Tidligere fraktur, menstruasjonsstatus, tid ved menarche er ikke relatert til tid til retur til idrett.12
Rehabilitering
Posteromediale tibia diafyse
Det er ikke konsensus i litteraturen med hensyn til varighet, MR-gradering og tidslinje for redusert belastning i rehabilitering av utøvere med stressreaksjon/fraktur i tibia. Rapportering av asymptomatiske pasienter med MR funn på stressreaksjon som ikke utvikler stressfraktur til tross for videre belastning understreker viktigheten av kontinuerlig klinisk vurdering. Det er varierende anbefalinger for retur til idrett på bakgrunn av radiologisk vs kliniske symptomer og retur til idrett.14
Forslag til rehabilitering av pasienter med stressreaksjon/fraktur ved posteromedial stressreaksjon/fraktur ved Olympiatoppen.
Basert på studier som er sammenlignbare med vår populasjon bør vi skissere forventet lengde på rehabilitering før retur til idrett ut fra MR gradering. Det er stor spredning i rapportert tid til retur til idrett, men øker vanligvis ved økende MR gradering. Resorpsjon kommer før beinmargsødemet, og selv lave graderinger vil derfor trenge relativt lang rehabiliteringstid.
Forventet tid til retur til idrett:
Grad 1 6-12 uker
Grad 2-4a: 12-16 uker
Grad 4b: 14-17+ uker
Disse tidsangivelsene er basert på de nyeste studiene. De er kun retningsgivende og vil variere fra pasient til pasient. Det må tas hensyn til risikofaktorer. Belastning styres strengt innenfor symptomgrensen.
Retningslinjer for rehabilitering
Fase 1:
Hovedmålet er å bli smertefri ved ADL. Pasienten kontrollerer all aktivitet basert på smerte. All aktivitet som involverer underekstremiteten skal være smertefri, det vil si 0 på en 0-10 smerteskala. Dersom pasienten har smerter ved normal gange skal det avlastes med krykker til han/hun kan gå uten symptomer.
Pasienten kan trene fritt i vann med svømming eller aquajogg. Øvelser med minimal vektbæring som ergometersykkel, ro/padle-ergometer kan gjennomføres dersom det er symptomfritt. Det må tas hensyn til energiforbruk ved REDs problematikk.
Forsøk på gange med belastning for å kontrollere for symptomer gjennomføres annenhver dag. Når pasienten kan gå normalt uten smerter seponeres krykkene. Dersom det skulle oppstå symptomer må pasienten over på krykkeavlastning igjen.
Overgang til fase 2 når pasienten har vært smertefri ved normal gange i 5 dager.
Fase 2:
Oppstart av lavbelastet aktivitet, både med hensyn til GRF og aktivering av leggmuskulatur.
Aktuelle øvelser i fase 2:
Trening i vann
Ergometersykkel
Ellipse- (bakover med progresjon til forover).
Stake-ergometer
Gange på flat tredemølle, progresjon til rask gange.
Når smertefri i øvelser med lav belastning, overgang til Alter-G mølle annenhver dag. Oppstart på 80% belastning på flat mølle. Progresjon med 5% intervall når pasienten har vært smertefri i 3 økter. Lav hastighet innledningsvis 8-9km/t, økende opp til 11 km/t før progresjon til neste belastningsnivå og lavere starthastighet.
Varighet av fase 2 er basert på forventet tidslinje, samt symptomfri i all aktivitet i 5 dager, inkludert smertefri løping på Alter-G med 95% belastning, 11 km/t.
Idrettsspesifikk styrketrening innenfor symptomgrenser.
Dersom pasienten ikke har tilgang på Alter-G mølle kan en bruke gå-jogg progresjon ad modum Warden.33 (se progresjon etter referanser)
Fase 3:
Pasienten skal ha vært smertefri gjennom progresjonen i fase 2, samt vært smertefri ved palpasjon av aktuelle område på tibia før progresjon til fase 3.
Oppstart med idrettsspesifikk trening annenhver dag. Kontroll av symptomer, som skal være 0/10.
Korte perioder med full belastning innen aktuelle idrett. Start med så lite som <5 min. Gradvis økende varighet.
Fase 4:
Overgang til ubegrenset idrettsaktivitet. I starten annenhver dag.
Vurdere 2 sykluser med 2 uker belastning og en uke med rolig belastning for å optimalisere i forhold til remodelleringsprosessen, ref Romani et al.
Øvrige tiltak:
Adressere risikofaktorer.
Teste ut bruk av pneumatisk ortose. Aktuelt dersom dette reduserer/eliminerer symptomer under trening. (Se evidens under andre tiltak).
Vurdere bruk av lavdosert ultralyd for grad 3. (Se evidens under andre tiltak).
Monitorering av smerte er viktig. Det er mulighet for daglig rapportering i Athletemonitoring for utøvere som er registrert i systemet.
Styrketrening
Det er vist en sammenheng mellom lavt muskelvolum i leggen og risiko for utvikling av stressfraktur. Det er også indikasjoner for at muskulær uttretting av leggmuskulatur under løping øker belastning på tibia. Vi bør diskutere treningstiltak med styrketrening for leggmuskulatur sammen med kraft/styrke. Nøkkelpunkter vil da være timing av øvelser i rehabiliteringsfasen, samt økt-sammensetning for volum og/eller utholdenhet og total belastning.
Anteriore tibia diafyse
Dette er en sjelden skade der stressreaksjonen/frakturen ligger på tensjonssiden av tibia. Den klassifiseres dermed som en høyrisiko skade, da det er større sannsynlighet for progresjon til komplett fraktur, delayed- eller non-union. For stressfrakturer på anteriore korteks anbefales konservativ behandling i opp til 6 mnd. Dersom utøveren fortsatt har symptomer etter 3-6 mnd, vurderes kirurgisk behandling. Tidligere ble margnagle brukt, men dagens kirurgi består av plate og skruer samt debridement av området.
Fredericson gradering 1-3 behandles med krykkeavlastning til pasienten kan gå uten smerter. Dersom begge kortikales er involvert, med komplett frakturlinje, behandles skaden som en akutt fraktur. Det er rapportert lavere rate for retur til idrett ved konservativ behandling vs kirurgisk behandling, 71% vs 96%. Rapportert tid til retur til idrett er lik for begge behandlingsmetoder. Ved konservativ behandling 3-14 måneder (gjennomsnitt 7 måneder), og kirurgisk 3-24 måneder (gjennomsnitt 7 måneder).34
Tid for retur til idrett er lengre enn ved posteromediale skader. Gjennomsnittstid for retur til idrett varierer fra 3-10 måneder, gjennomsnitt 7 måneder.1
Tibiaplatå
Stressfrakturer på tibiaplatået oppstår medialt og posteriort. Det er lite litteratur som tar for seg rehabiliterings tiltak og tidsaspekt, og studiene er gamle. Studiene indikerer retur til full aktivitet etter 12-20 uker fra diagnosetidspunkt.35 De behandles etter samme retningslinjer som for stressfrakturer i posteromediale korteks.
Andre tiltak
Pneumatisk ortose
Det er rapportert betydelig kortere tid til retur til idrett ved bruk av pneumatisk ortose i flere studier. De fleste av disse er fra 90-tallet og av lav vitenskapelig kvalitet. Et unntak er randomisert studie av Swenson et al36 som viste kortere tid til trening med lav belastning, og kortere tid til smertefri hink-belastning. Studien brukte bone scan som undersøkelse og skadene er derfor ikke gradert.
To nyere studie på militært personell fant ingen signifikant effekt av ortose i forhold til kontrollgruppen på tibiale stressfrakturer.37,38 En systematisk review, som også inkluderte tidligere nevnte studier med lav kvalitet, konkluderte med 1 måneds kortere tid til retur til idrett ved bruk av ortose.34
Det er foreløpig ikke studier som gjør det mulig å trekke noe konklusjon med hensyn til effekt av ortose. Det er imidlertid et billig tiltak, og bør vurderes for våre pasienter med påvist stressreaksjon/fraktur i posteromediale del av tibia.
LIPUS (Low Intensity Pulsed Ultrasound)
En systematisk review fra 2017 konkluderer med at det er noe effekt av behandling med LIPUS for ferske frakturer. Det har ingen effekt på utfallsmål som er viktige for pasienten, og sannsynligvis ingen effekt på radiologisk beintilheling. For andre typer frakturer er det åpent for debatt.39 For pasienter som er operert med fiksasjon har LIPUS ingen effekt på radiografisk tilheling eller raskere funksjonell bedring.40
Det er gjort få studier på effekt av LIPUS ved behandling av stressfrakturer. Studier som har høy risiko for bias viser større effekt. Studier med høy pasient compliance viser også større effekt.41
En dobbelt blindet, randomisert, placebo kontrollert studie fant at LIPUS ikke var effektiv med hensyn til radiologisk tilheling ved stressfrakturer i tibia. De fant ingen endring i MR gradering etter 12 uker. De brukte kun 4 uker LIPUS stimulering.23
Yadav et al gjorde en dobbelt blindet, randomisert, placebo kontrollert studie og fant at behandling med LIPUS ga kortere tid til retur til tjeneste for militært personell (25 dager i LIPUS gruppen, og 40 dager i placebogruppen). Pasientene brukte LIPUS 10 minutter daglig. Det ble ikke kontrollert for radiologisk tilheling. Det ble brukt bone scanning i diagnosen og skadene ble derfor ikke klassifisert.42
Rue et al gjorde også en dobbelt blindet, randomisert, placebo kontrollert studie og fant at behandling med LIPUS ikke viste signifikante forskjeller med hensyn til retur til idrett og radiologisk tilheling. Pasientene ble ikke klassifisert, men vanligste funn var periosteal reaksjon. Pasientene brukte LIPUS 20 minutter daglig til de var smertefrie, og det var tegn til radiologisk tilheling på røntgen ved 8 uker for begge gruppene. Det var en forsinkelse fra diagnose til intervensjon på gjennomsnittlig 29 dager som kan ha påvirket resultatene.23
Det er lite evidens for effekten av LIPUS på stressfrakturer. Vi har behandlingsapparater tilgjengelig på Olympiatoppen og bør vurdere å bruke dette på stipendutøvere som er gradert til 3 og 4 på Fredericsons gradering. Behandlingen bør da startes så tidlig som mulig, og fortsette til retur til idrett.
Referanser
1 Robertson, G. A. & Wood, A. M. Return to sports after stress fractures of the tibial diaphysis: a systematic review. British medical bulletin 114, 95-111, doi:10.1093/bmb/ldv006 (2015).
2 Milner, C. E., Ferber, R., Pollard, C. D., Hamill, J. & Davis, I. S. Biomechanical factors associated with tibial stress fracture in female runners. Med Sci Sports Exerc 38, 323-328, doi:10.1249/01.mss.0000183477.75808.92 (2006).
3 Rue, J. P., Armstrong, D. W., 3rd, Frassica, F. J., Deafenbaugh, M. & Wilckens, J. H. The effect of pulsed ultrasound in the treatment of tibial stress fractures. Orthopedics 27, 1192-1195 (2004).
4 Boden, B. P., Osbahr, D. C. & Jimenez, C. Low-risk stress fractures. Am J Sports Med 29, 100-111, doi:10.1177/03635465010290010201 (2001).
5 Harris, C. E., 3rd, Vincent, H. K. & Vincent, K. R. Sacral Stress Fractures: They See You, But Are You Seeing Them? Curr Sports Med Rep 15, 73, doi:10.1249/JSR.0000000000000245 (2016).
6 Romani, W. A., Gieck, J. H., Perrin, D. H., Saliba, E. N. & Kahler, D. M. Mechanisms and management of stress fractures in physically active persons. Journal of athletic training 37, 306-314 (2002).
7 Robling, A. G., Castillo, A. B. & Turner, C. H. Biomechanical and molecular regulation of bone remodeling. Annual review of biomedical engineering 8, 455-498, doi:10.1146/annurev.bioeng.8.061505.095721 (2006).
8 Matijevich, E. S., Branscombe, L. M., Scott, L. R. & Zelik, K. E. Ground reaction force metrics are not strongly correlated with tibial bone load when running across speeds and slopes: Implications for science, sport and wearable tech. PloS one 14, e0210000, doi:10.1371/journal.pone.0210000 (2019).
9 Rice, H. W., G; Trudeau, MB; et al. Estimating tibial stress throughout the duration of a treadmill run. (2019).
10 Diehl, J. J., Best, T. M. & Kaeding, C. C. Classification and return-to-play considerations for stress fractures. Clin Sports Med 25, 17-28, vii, doi:10.1016/j.csm.2005.08.012 (2006).
11 Jensen, R., Leissring, SK, Stephenson, ML. 33rd International Conference on Biomechanics in Sports (2015).
12 Nattiv, A. et al. Correlation of MRI grading of bone stress injuries with clinical risk factors and return to play: a 5-year prospective study in collegiate track and field athletes. Am J Sports Med 41, 1930-1941, doi:10.1177/0363546513490645 (2013).
13 Kenkre, J. S. & Bassett, J. The bone remodelling cycle. Annals of clinical biochemistry 55, 308-327, doi:10.1177/0004563218759371 (2018).
14 Feldman, J. J., Bowman, E. N., Phillips, B. B. & Weinlein, J. C. Tibial Stress Fractures in Athletes. The Orthopedic clinics of North America 47, 733-741, doi:10.1016/j.ocl.2016.05.015 (2016).
15 Yukata, K. et al. Medial tibial plateau morphology and stress fracture location: A magnetic resonance imaging study. World journal of orthopedics 8, 484-490, doi:10.5312/wjo.v8.i6.484 (2017).
16 Winters, M. et al. Medial tibial stress syndrome can be diagnosed reliably using history and physical examination. Br J Sports Med 52, 1267-1272, doi:10.1136/bjsports-2016-097037 (2018).
17 Beck, B. R. et al. Tibial stress injury: relationship of radiographic, nuclear medicine bone scanning, MR imaging, and CT Severity grades to clinical severity and time to healing. Radiology 263, 811-818, doi:10.1148/radiol.12102426 (2012).
18 Miller, T. L., Jamieson, M., Everson, S. & Siegel, C. Expected Time to Return to Athletic Participation After Stress Fracture in Division I Collegiate Athletes. Sports health 10, 340-344, doi:10.1177/1941738117747868 (2018).
19 Jamieson, M. et al. Time to return to running after tibial stress fracture in female Division I collegiate track and field. 28, 393-397, doi:10.1097/bco.0000000000000524 (2017).
20 Arendt, E., Agel, J., Heikes, C. & Griffiths, H. Stress injuries to bone in college athletes: a retrospective review of experience at a single institution. Am J Sports Med 31, 959-968, doi:10.1177/03635465030310063601 (2003).
21 Dobrindt, O. et al. Estimation of return-to-sports-time for athletes with stress fracture - An approach combining risk level of fracture site with severity based on imaging. BMC musculoskeletal disorders 13, 139, doi:10.1186/1471-2474-13-139 (2012).
22 Kijowski, R., Choi, J., Shinki, K., Del Rio, A. M. & De Smet, A. Validation of MRI classification system for tibial stress injuries. AJR. American journal of roentgenology 198, 878-884, doi:10.2214/AJR.11.6826 (2012).
23 Gan, T. Y., Kuah, D. E., Graham, K. S. & Markson, G. Low-Intensity Pulsed Ultrasound in Lower Limb Bone Stress Injuries: A Randomized Controlled Trial. Clinical Journal of Sport Medicine 24, 457-460, doi:10.1097/jsm.0000000000000084 (2014).
24 Bergman, A. G., Fredericson, M., Ho, C. & Matheson, G. O. Asymptomatic Tibial Stress Reactions: MRI Detection and Clinical Follow-Up in Distance Runners. American Journal of Roentgenology 183, 635-638, doi:10.2214/ajr.183.3.1830635 (2004).
25 Fredericson, M., Bergman, A. G., Hoffman, K. L. & Dillingham, M. S. Tibial stress reaction in runners. Correlation of clinical symptoms and scintigraphy with a new magnetic resonance imaging grading system. Am J Sports Med 23, 472-481, doi:10.1177/036354659502300418 (1995).
26 Arendt, E. A. & Griffiths, H. J. The use of MR imaging in the assessment and clinical management of stress reactions of bone in high-performance athletes. Clin Sports Med 16, 291-306 (1997).
27 Geusens, P., Emans, P. J., de Jong, J. J. & van den Bergh, J. NSAIDs and fracture healing. Current opinion in rheumatology 25, 524-531, doi:10.1097/BOR.0b013e32836200b8 (2013).
28 Dimmen, S., Nordsletten, L., Engebretsen, L., Steen, H. & Madsen, J. E. Negative effect of parecoxib on bone mineral during fracture healing in rats. Acta orthopaedica 79, 438-444, doi:10.1080/17453670710015373 (2008).
29 Thein-Nissenbaum, J. & Hammer, E. Treatment strategies for the female athlete triad in the adolescent athlete: current perspectives. Open Access J Sports Med 8, 85-95, doi:10.2147/OAJSM.S100026 (2017).
30 Mountjoy, M. et al. The IOC consensus statement: beyond the Female Athlete Triad--Relative Energy Deficiency in Sport (RED-S). Br J Sports Med 48, 491-497, doi:10.1136/bjsports-2014-093502 (2014).
31 Ackerman, K. E., Skrinar, G. S., Medvedova, E., Misra, M. & Miller, K. K. Estradiol levels predict bone mineral density in male collegiate athletes: a pilot study. Clin Endocrinol (Oxf) 76, 339-345, doi:10.1111/j.1365-2265.2011.04212.x (2012).
32 Giffin, K. L., Knight, K. B., Bass, M. A. & Valliant, M. W. Predisposing Risk Factors and Stress Fractures in Division I Cross Country Runners. J Strength Cond Res, doi:10.1519/jsc.0000000000002408 (2017).
33 Warden, S. J., Davis, I. S. & Fredericson, M. Management and prevention of bone stress injuries in long-distance runners. The Journal of orthopaedic and sports physical therapy 44, 749-765, doi:10.2519/jospt.2014.5334 (2014).
34 Robertson, G. A. & Wood, A. M. Lower limb stress fractures in sport: Optimising their management and outcome. World journal of orthopedics 8, 242-255, doi:10.5312/wjo.v8.i3.242 (2017).
35 Rosenthal, M. D., Moore, J. H. & DeBerardino, T. M. Diagnosis of medial knee pain: atypical stress fracture about the knee joint. The Journal of orthopaedic and sports physical therapy 36, 526-534, doi:10.2519/jospt.2006.2125 (2006).
36 Swenson, E. J., Jr. et al. The effect of a pneumatic leg brace on return to play in athletes with tibial stress fractures.Am J Sports Med 25, 322-328, doi:10.1177/036354659702500309 (1997).
37 Allen, C. S. et al. The use of a pneumatic leg brace in soldiers with tibial stress fractures--a randomized clinical trial. Military medicine 169, 880-884 (2004).
38 Moen, M. H. et al. The additional value of a pneumatic leg brace in the treatment of recruits with medial tibial stress syndrome; a randomized study. Journal of the Royal Army Medical Corps 156, 236-240 (2010).
39 Schandelmaier, S. et al. Low intensity pulsed ultrasound for bone healing: systematic review of randomized controlled trials. Bmj 356, j656, doi:10.1136/bmj.j656 (2017).
40 Busse, J. W. et al. Re-evaluation of low intensity pulsed ultrasound in treatment of tibial fractures (TRUST): randomized clinical trial. Bmj 355, i5351, doi:10.1136/bmj.i5351 (2016).
41 Busse, J. W. et al. Trial to re-evaluate ultrasound in the treatment of tibial fractures (TRUST): a multicenter randomized pilot study. Trials 15, 206, doi:10.1186/1745-6215-15-206 (2014).
42 Yadav, Y. K., Salgotra, K. R. & Banerjee, A. Role of Ultrasound Therapy in the Healing of Tibial Stress Fractures. Medical journal, Armed Forces India 64, 234-236, doi:10.1016/S0377-1237(08)80101-3 (2008).
Gå- jogg progresjon a.m. Warden33:
|
Løpsprogresjon retur til idrettsfase stressfraktur tibia |
|||
|
All trening skal være smertefri. |
|||
|
Uke 1 |
Gå 9 minutter |
Jogge 1 min |
x 3 |
|
|
Hviledag |
|
|
|
|
Gå 8 minutter |
Jogge 2 min |
x 3 |
|
|
Hviledag |
|
|
|
|
Gå 7 minutter |
Jogge 3 min |
x 3 |
|
|
2 hviledager |
|
|
|
Uke 2 |
Gå 6 minutter |
Jogge 4 min |
x 3 |
|
|
Hviledag |
|
|
|
|
Gå 5 minutter |
Jogge 5 min |
x 3 |
|
|
Hviledag |
|
|
|
|
Gå 4 minutter |
Jogge 6 min |
x 3 |
|
|
2 hviledager |
|
|
|
Uke 3 |
Gå 2 minutter |
Jogge 8 min |
x 3 |
|
|
Hviledag |
|
|
|
|
Gå 2 minutter |
Jogge 8 min |
x 3 |
|
|
Hviledag |
|
|
|
|
Gå 2 minutter |
Jogge 8 min |
x 3 |
|
|
2 hviledager |
|
|
|
Uke 4 |
Jogge 30 min |
|
|
|
|
Hviledag |
|
|
|
|
Løpe 30 min 60% av normal hastighet |
|
|
|
|
Hviledag |
|
|
|
|
Løpe 30 min 70% av normal hastighet |
|
|
|
|
2 hviledager |
|
|
|
Uke 5 |
Løpe 30 min 80% av normal hastighet |
|
|
|
|
Hviledag |
|
|
|
|
Løpe 30 min 90% av normal hastighet |
|
|
|
|
Hviledag |
|
|
|
|
Løpe 30 min |
|
|
|
|
2 hviledager |
|
|
|
Uke 6 |
Løp 30 min normal hastighet |
|
|
|
|
Løp 30 min normal hastighet |
|
|
|
|
Hviledag |
|
|
|
|
Løp 30 min normal hastighet |
|
|
|
|
Løp 30 min normal hastighet |
|
|
|
|
2 hviledager |
|
|
|
Uke 7 |
Tilbake til normal trening i 2 uker etterfulgt av en rolig uke |
|
|
|
|
(repeter denne syklussen 2 ganger (2 harde uker etterfulgt av en rolig uke) |
|
|